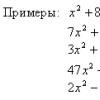ОПРЕДЕЛЕНИЕ
Химическими реакция называют превращения веществ, в которых происходит изменение их состава и (или) строения.
Наиболее часто под химическими реакциями понимают процесс превращения исходных веществ (реагентов) в конечные вещества (продукты).
Химические реакции записываются с помощью химических уравнений, содержащих формулы исходных веществ и продуктов реакции. Согласно закону сохранения массы, число атомов каждого элемента в левой и правой частях химического уравнения одинаково. Обычно формулы исходных веществ записывают в левой части уравнения, а формулы продуктов – в правой. Равенство числа атомов каждого элемента в левой и правой частях уравнения достигается расстановкой перед формулами веществ целочисленных стехиометрических коэффициентов.
Химические уравнения могут содержать дополнительные сведения об особенностях протекания реакции: температура, давление, излучение и т.д., что указывается соответствующим символом над (или «под») знаком равенства.
Все химические реакции могут быть сгруппированы в несколько классов, которым присущи определенные признаки.
Классификация химических реакций по числу и составу исходных и образующихся веществ
Согласно этой классификации, химические реакции подразделяются на реакции соединения, разложения, замещения, обмена.
В результате реакций соединения из двух или более (сложных или простых) веществ образуется одно новое вещество. В общем виде уравнение такой химической реакции будет выглядеть следующим образом:
Например:
СаСО 3 + СО 2 + Н 2 О = Са(НСО 3) 2
SO 3 + H 2 O = H 2 SO 4
2Mg + O 2 = 2MgO.
2FеСl 2 + Сl 2 = 2FеСl 3
Реакции соединения в большинстве случаев экзотермические, т.е. протекают с выделением тепла. Если в реакции участвуют простые вещества, то такие реакции чаще всего являются окислительно-восстановительными (ОВР), т.е. протекают с изменением степеней окисления элементов. Однозначно сказать будет ли реакция соединения между сложными веществами относиться к ОВР нельзя.
Реакции, в результате которых из одного сложного вещества образуется несколько других новых веществ (сложных или простых) относят к реакциям разложения . В общем виде уравнение химической реакции разложения будет выглядеть следующим образом:
Например:
CaCO 3 CaO + CO 2 (1)
2H 2 O =2H 2 + O 2 (2)
CuSO 4 × 5H 2 O = CuSO 4 + 5H 2 O (3)
Cu(OH) 2 = CuO + H 2 O (4)
H 2 SiO 3 = SiO 2 + H 2 O (5)
2SO 3 =2SO 2 + O 2 (6)
(NH 4) 2 Cr 2 O 7 = Cr 2 O 3 + N 2 +4H 2 O (7)
Большинство реакций разложения протекает при нагревании (1,4,5). Возможно разложение под действием электрического тока (2). Разложение кристаллогидратов, кислот, оснований и солей кислородсодержащих кислот (1, 3, 4, 5, 7) протекает без изменения степеней окисления элементов, т.е. эти реакции не относятся к ОВР. К ОВР реакциям разложения относится разложение оксидов, кислот и солей, образованных элементами в высших степенях окисления (6).
Реакции разложения встречаются и в органической химии, но под другими названиями — крекинг (8), дегидрирование (9):
С 18 H 38 = С 9 H 18 + С 9 H 20 (8)
C 4 H 10 = C 4 H 6 + 2H 2 (9)
При реакциях замещения простое вещество взаимодействует со сложным, образуя новое простое и новое сложное вещество. В общем виде уравнение химической реакции замещения будет выглядеть следующим образом:
Например:
2Аl + Fe 2 O 3 = 2Fе + Аl 2 О 3 (1)
Zn + 2НСl = ZnСl 2 + Н 2 (2)
2КВr + Сl 2 = 2КСl + Вr 2 (3)
2КСlO 3 + l 2 = 2KlO 3 + Сl 2 (4)
СаСО 3 + SiO 2 = СаSiO 3 + СО 2 (5)
Са 3 (РО 4) 2 + ЗSiO 2 = ЗСаSiO 3 + Р 2 О 5 (6)
СН 4 + Сl 2 = СН 3 Сl + НСl (7)
Реакции замещения в своем большинстве являются окислительно-восстановительными (1 – 4, 7). Примеры реакций разложения, в которых не происходит изменения степеней окисления немногочисленны (5, 6).
Реакциями обмена называют реакции, протекающие между сложными веществами, при которых они обмениваются своими составными частями. Обычно этот термин применяют для реакций с участием ионов, находящихся в водном растворе. В общем виде уравнение химической реакции обмена будет выглядеть следующим образом:
АВ + СD = АD + СВ
Например:
CuO + 2HCl = CuCl 2 + H 2 O (1)
NaOH + HCl = NaCl + H 2 O (2)
NаНСО 3 + НСl = NаСl + Н 2 О + СО 2 (3)
AgNО 3 + КВr = АgВr ↓ + КNО 3 (4)
СrСl 3 + ЗNаОН = Сr(ОН) 3 ↓+ ЗNаСl (5)
Реакции обмена не являются окислительно-восстановительными. Частный случай этих реакций обмена -реакции нейтрализации (реакции взаимодействия кислот со щелочами) (2). Реакции обмена протекают в том направлении, где хотя бы одно из веществ удаляется из сферы реакции в виде газообразного вещества (3), осадка (4, 5) или малодиссоциирующего соединения, чаще всего воды (1, 2).
Классификация химических реакций по изменениям степеней окисления
В зависимости от изменения степеней окисления элементов, входящих в состав реагентов и продуктов реакции все химические реакции подразделяются на окислительно-восстановительные (1, 2) и, протекающие без изменения степени окисления (3, 4).
2Mg + CO 2 = 2MgO + C (1)
Mg 0 – 2e = Mg 2+ (восстановитель)
С 4+ + 4e = C 0 (окислитель)
FeS 2 + 8HNO 3 (конц) = Fe(NO 3) 3 + 5NO + 2H 2 SO 4 + 2H 2 O (2)
Fe 2+ -e = Fe 3+ (восстановитель)
N 5+ +3e = N 2+ (окислитель)
AgNO 3 +HCl = AgCl ↓ + HNO 3 (3)
Ca(OH) 2 + H 2 SO 4 = CaSO 4 ↓ + H 2 O (4)
Классификация химических реакций по тепловому эффекту
В зависимости от того, выделяется ли или поглощается тепло (энергия) в ходе реакции, все химические реакции условно разделяют на экзо – (1, 2) и эндотермические (3), соответственно. Количество тепла (энергии), выделившееся или поглотившееся в ходе реакции называют тепловым эффектом реакции. Если в уравнении указано количество выделившейся или поглощенной теплоты, то такие уравнения называются термохимическими.
N 2 + 3H 2 = 2NH 3 +46,2 кДж (1)
2Mg + O 2 = 2MgO + 602, 5 кДж (2)
N 2 + O 2 = 2NO – 90,4 кДж (3)
Классификация химических реакций по направлению протекания реакции
По направлению протекания реакции различают обратимые (химические процессы, продукты которых способны реагировать друг с другом в тех же условиях, в которых они получены, с образованием исходных веществ) и необратимые (химические процессы, продукты которых не способны реагировать друг с другом с образованием исходных веществ).
Для обратимых реакций уравнение в общем виде принято записывать следующим образом:
А + В ↔ АВ
Например:
СН 3 СООН + С 2 Н 5 ОН↔ Н 3 СООС 2 Н 5 + Н 2 О
Примерами необратимых реакций может служить следующие реакции:
2КСlО 3 → 2КСl + ЗО 2
С 6 Н 12 О 6 + 6О 2 → 6СО 2 + 6Н 2 О
Свидетельством необратимости реакции может служить выделение в качестве продуктов реакции газообразного вещества, осадка или малодиссоциирующего соединения, чаще всего воды.
Классификация химических реакций по наличию катализатора
С этой точи зрения выделяют каталитические и некаталитические реакции.
Катализатором называют вещество, ускоряющее ход химической реакции. Реакции, протекающие с участием катализаторов, называются каталитическими. Протекание некоторых реакций вообще невозможно без присутствия катализатора:
2H 2 O 2 = 2H 2 O + O 2 (катализатор MnO 2)
Нередко один из продуктов реакции служит катализатором, ускоряющим эту реакцию (автокаталитические реакции):
MeO+ 2HF = MeF 2 + H 2 O, где Ме – металл.
Примеры решения задач
ПРИМЕР 1
Внимание! Администрация сайта сайт не несет ответственности за содержание методических разработок, а также за соответствие разработки ФГОС.
Победитель конкурса "Электронный учебник на уроке".
7-й класс
Цель урока:
- изучение и первичное осознание химических явлений; выяснение признаков и условий протекания химических реакций;
- совершенствование умения отличать физические процессы от химических; формирование практических навыков при работе с химическими реактивами и лабораторным оборудованием.
Задачи урока:
образовательные:
- закрепить знания учащихся о физических и химических явлениях;
- содействовать формированию у учащихся знаний о признаках и условиях протекания химических реакций;
развивающие:
- развивать умение ставить проблемы и решать их, устанавливать межпредметные связи;
- вырабатывать практические умения работать с лабораторным оборудованием и реактивами в соответствии с правилами по ТБ;
- продолжать формирование умений оформлять результаты учебного эксперимента;
- развивать способность к само- и взаимоконтролю.
воспитательные:
- воспитывать культуру общения через работу в парах;
- продолжить формирование представлений о положительной роли химии для объяснения происходящих процессов в природе и в организме человека.
Тип урока: урок изучения и первичного закрепления знаний.
Методы обучения: беседа, рассказ учителя, демонстрационный эксперимент, демонстрация видеофрагментов, использование ЭФУ.
Оборудование: ПК, медиапроектор, наборы для лабораторной работы, рабочая тетрадь.
Средства обучения: мультимедийная презентация.
Этапы урока
- Деятельность учителя
- Деятельность ученика
- Примечание
Ход урока
I. Организационный момент – 1 мин
В течение урока вам предстоит работать с электронными приложениями Я надеюсь, что урок будет интересным и полезным для вас.
Цель: создание положительного эмоционального настроя на усвоение учебного материала, формулирование целей и задач урока, ожидаемых результатов.
II. Проверка домашнего задания – 5 мин
– Ребята, какие явления могут встречаться в нашей жизни?
– Как вы считаете, какие из этих явлений должна изучать физика, а какие - химия?
– Сформулируйте определения физических и химических явлений.
– Химия – одна из наук, помогающая познать тайны природы. Но этому надо учиться. Одно из необходимых умений – это умение наблюдать явлений, отличать, определять принадлежность явления к определенной группе. На экране будут представлены картинки физических и химических явлений.
Физическое явление – это явление, при котором, изменяется агрегатное состояние вещества или форма образованного им тела, а само вещество остаётся без изменений.
Химическое явление – это явление, при котором одно вещество превращается в другое.
III. Мотивация к открытию новых знаний – 2 мин
Скажите, теперь вы сможете отличить физическое явление от химической реакции?
– Достаточно ли ваших знаний для этого?
– Какой главный отличительный признак химической реакции?
– Ежеминутно в мире протекает миллионы химических реакций – в нашем желудке, когда мы едим, в выпекающемся пироге или в двигателе автомобиля. Но как определить происходит химическая реакция или нет?
При химических процессах происходит превращение одних веществ в другие, которые обладают новыми свойствами, которыми не обладали исходные вещества. Эти превращения сопровождаются яркими и наглядными изменениями. Эти наглядные изменения называются признаки.
– Что ещё вам необходимо знать о химических реакциях, чтобы безошибочно отличать их от физических явлений?
– Поэтому какую тему мы будем изучать сегодня на уроке?
– Должно быть что-то очень заметное
– Знать признаки химический явлений (реакций)
– Признаки химических реакций
Цель: подготовка к осознанному восприятию материала, стимулирование познавательного интереса.
IV. Актуализация субъектного опыта учащихся – 3 мин
“Химии никоим образом научиться невозможно, не видав самой практики и не принимаясь за химические операции”.
М.В. Ломоносов
– Как вы понимаете эти слова?
– Что хотели бы узнать и чему научиться на уроке:
- выявить – (признаки химических реакций)
- определить – (отличия химических и физических явлений)
- познакомиться – (с условиями протекания реакций)
- провести – (химический эксперимент)
- отметить – (значение химических реакций)
Главный признак химической реакции – это образование новых веществ с новыми свойствами. Вы знаете много веществ, но ваши знания будут неполными, если мы не изучим явления происходящие с ними. Вот по этому, сегодня на уроке вы должны провести различные реакции и выяснить их основные признаки.
– Для того чтобы проводить опыты, нужно знать какие вещества необходимо брать для реакции.
(учащиеся формируют цели урока)
Цель: активизация личного опыта каждого ученика и использование его в обучении, подготовка к восприятию нового материала, оценка учителем уровня подготовленности учащихся.
V. Открытие новых знаний, изучение нового материала (лабораторный эксперимент) – 12 мин
– В ходе исследования вы будете выступать в роли юных химиков – экспериментаторов. Нам предстоит работать с реактивами, в том числе с кислотами и щелочами. Вспомните правила ТБ, которые необходимо знать при работе с этими веществами.
– Анализируя лабораторный эксперимент, не забывайте записывать свои наблюдения в рабочую тетрадь и делать выводы. Пользоваться можно глазами, руками, памятью, эрудицией, правилами техники безопасности и реактивами.
– Какие опыты проводили и какие признаки наблюдали?
– Как вы думаете, какие условия необходимо выполнить, чтобы произошла химическая реакция?
(ребята перечисляют правила ТБ)
Условия протекания химических реакций: соприкосновение веществ, нагревание
Цель: формирование новых знаний о химических реакциях, признаках, условиях протекания реакции и классификации реакций по тепловому эффекту.
VI. Закрепление изученного – 5 мин
Используя электронные приложения, ребята закрепляют изученный материал.
– Прочитайте описание явлений и укажите, в какой части текста говориться о физическом явлении, а в какой о химической реакции. Назовите признаки химической реакции.
1) При горении свечи воск сначала плавится и смачивает фитиль, а потом сгорает, образуя углекислый газ и пары воды. Горение сопровождается образованием пламени.
2) В процессе выплавки чугуна из руды образуется металл. Горячий чугун разливают в формы, в которых он постепенно остывает и затвердевает.
3) Для приготовления лимонада в воду высыпают кристаллики лимонной кислоты. Они постепенно растворяются. Затем в воду с кислотой добавляют соду. В результате появляются пузырьки газа.
4) При нагревании воды она испаряется, а при действии на неё электрического тока, воды разлагается на два простых газообразных вещества: кислород и водород.
5) При длительном пережёвывании чёрного хлеба он измельчается. Потом вы почувствуете сладковатый вкус, так как хлеб начинает перевариваться под действием слюны.
6) Для приготовления теста сначала дрожжи растворяют в воде. Затем их добавляют к остальным компонентам теста. В результате появляются пузырьки газа, которые делают тесто воздушным.
– Итак, запишем в рабочую тетрадь признаки и условия протекания реакций
Плавление воска - физическое явление, т.к. меняется его агрегатное состояние, а горение - химическое, в тексте говорится об образовании двух новых веществ.
Превращение руды в чугун – процесс химический, а остывание и затвердевание чугуна - физический.
Растворение кристалликов лимонной кислоты – явление физическое, т.к. меняется размер частиц вещества. После добавления соды произошла химическая реакция – как появляются пузырьки какого-то нового вещества.
Испарение воды – физическое явление, так как меняется агрегатное состояние вещества, а разложение под действием тока - химическое, так как образовались новые вещества.
Измельчение хлеба - физическое явление. Переваривание под действием слюны - химическое.
1-2 минуты дети знакомятся с текстом и обсуждают его. Учитель направляет обсуждение ответов каждой группы остальными детьми.
Включить экран.
VII. Применение изученного – 3 мин
– Молодцы, ребята! Вы на практике узнали о некоторых признаках химических реакций. Но... вся ли информация сейчас прозвучала? Как вы думаете?
– Совершенно верно! Мы ничего не сказали о том, где человек в своей повседневной жизни может встретиться с химическими реакциями и наблюдать за их признаками, какие химические реакции происходят в природе и какими признаками они сопровождаются. Можете привести примеры?
– Наверно, не вся!
– Извержения вулканов. Огромное количество (выделение энергии в виде тепла и света)
– Летом листья на деревьях зелёные, а осенью жёлтые и красные
– Образование пещер, т.к. происходит взаимодействие таких минералов, как известняк, с водой и углекислым газом, что приводит к их растворению?
VIII. Контроль и самоконтроль – 5 мин
1. Установите соответствие
Явления : 1). Растворение соли в воде; 2). Плавление свинца; 3). Загнивание белка; 4). Почернение серебряной ложки.
Название явления: а). Физическое явление; б) Химическое явление.
(1а; 2а; 3б; 4б).
2. Укажите признаки следующих химических реакций
Название химической реакции.
Признак хим. реакции.
- Прокисание молока.
- Горение бензина.
- Разложение сахара.
- Образование накипи в чайнике.
- Открывание бутылки с газированной водой
– Ваше время закончилось. Проверьте свои ответы и выставьте себе оценки. .
Цель: репродуктивное воссоздание изученного материала, систематизация и обобщение, выполнение заданий на изученную тему, первичная проверка усвоения и понимания материала.
IX. Домашнее задание – 1 мин
Приведите пословицы, где речь идёт о явлениях. Определите группу явлений: физические или химические
Цель: разъяснение, постановка домашнего задания.
X. Подведение итогов. Рефлексия – 2 мин
– В ходе урока вы попытались овладеть самым главным в процессе познания – умением находить истину с помощью доказательств, то есть проводить исследования. Многие учёные прошлых веков опирались в своих изысканиях лишь на интуицию и в результате нередко ошибались. Вы же с помощью опытов нашли свою истину.
Без химических реакций невозможна жизнь и все многообразие веществ. И задача человека, изучив этот мир, постараться использовать полученные знания во благо.
Продолжите предложение:
- Теперь я знаю, что...
- Теперь я знаю, как...
- Теперь я умею...
- Меня удивило...
– Выразите свое мнение об уроке, выбрав смайлик.
– Что ещё вы хотели бы знать о химических реакциях?
– В заключение я хочу сказать, что химия – это удивительная наука, вы ее только начинаете познавать. Спасибо за сотрудничество.
1. Химические реакции. Признаки и условия их протекания. Химические уравнения. Закон сохранения массы веществ. Типы химических реакций.
2. Какой объем газа можно получить при взаимодействии 60г, 12% раствора карбоната калия с серной кислотой.
Химическая реакция
- превращение одного или нескольких веществ в другое.
Типы химических реакций:
1)Реакция соединения
– это реакции в результате которых из двух веществ образуется одно более сложное.
2)Реакция разложения
- это реакция в результате которых из одного сложного вещества образуется несколько более простых.
3)Реакция замещения
– это реакции между простым и сложным веществами, в результате которых образуется новое простое и новое сложное вещество.
4)Реакция обмена
– это реакции между двумя сложными веществами, в результате которых они обмениваются своими составными частями.
Условия протекания реакции:
1)Тесное соприкосновение веществ.
2)Нагревание
3)Измельчённость (быстрее всего идут реакции в растворах)
Любая химическая реакция может быть изображена с помощью химического уравнения.
Химическое уравнение – это условная запись химической реакции с помощью химических формул и коэфицентов.
В основе химических уравнений лежит закон сохранения массы вещества
: массы веществ вступивших в реакцию равна массе веществ получившихся в результате реакции.
Признаки химических реакций:
· Изменение окраски
· Выделение газа
· Выпадение осадка
· Выделение тепла и света
· Выделение запаха
2.

Билет №7
1. Основные положения Т.Э.Д. – теория электрической диссоциации.
2. Сколько грамм магния, содержащего 8% примесей, может прореагировать с 40г соляной кислоты.
Вещества, растворимые в воде могут диссоциировать, т.е. распадаться на противоположно заряженные ионы.
Электрическая диссоциация
–
распад электролита на ионы при растворении или расплавлении.
Электролиты
–
вещества, растворы или расплавы которых проводят электрический ток (кислоты, соли, щелочи).
Они образованы ионной связью (соли, щелочи), или ковалентной,сильнополярной (кислоты).
Не электролиты
–
вещества, растворы которых не проводят электрический ток (раствор сахара, спирта, глюкозы)
При диссоциации электролиты распадаются на катионы(+)
ианионы(-)
Ионы –
заряженные частица, в которые превращаются атомы, в результате отдатия и взятия ē
Химические свойства растворов электролитов определяются свойствами тех ионов, которые образуются при диссоциации.

Кислота
– электролит, который диссоциирует на катионы водорода и анион кислотного остатка.
Серная кислота диссоциирует на 2 катиона Н с зарядом (+) и
анион SO 4 с зарядои (-)
Основания
– электролит, который диссоциирует на катионы металла и гидроксид анионы.
Соли – электролит, который в водном растворе диссоциирует на катионы металла и анионы кислотного остатка.
2.
1. Реакции ионного обмена.
Тема урока . Практическая работа №4 «Признаки химических реакций»
Цель обучающая:
Совершенствовать знания о признаках химических реакций;
Совершенствовать экспериментальные умения:
Определять цель работы;
Пользоваться инструкцией и лабораторным оборудованием ;
Проводить реакции;
Наблюдать и фиксировать наблюдения;
Записывать уравнения реакций согласно эксперименту;
Делать выводы на основе наблюдений согласно поставленной цели;
Соблюдать правила безопасного поведения Цель развивающая:
Развивать навыки самостоятельной работы, коммуникативные навыки. Цель воспитательная:
Воспитание аккуратности и последовательности в работе, бережного отношения к школьному имуществу, собственному здоровью и здоровью окружающих.
На столах учащихся.
Реактивы: оксид меди (II), серная кислота, мел, соляная кислота, хлорид железа (III), роданид калия, карбонат натрия, хлорид кальция.
Оборудование: штатив лабораторный, пробирки, спиртовка, спички
Дидактические материалы: инструкционные карточки, тест и бланки для ответов на тесты.
Эпиграф к уроку «Чтобы познать невидимое, смотри внимательно на видимое» Древняя мудрость
Этап | Деятельность | Формы работы |
||
учителя | учащихся |
|||
Мотивация, целеполага-ние | Предлагаем учащимся записать тему урока и высказать идеи относительно целей, которые нам предстоит реализовать на уроке. Далее побуждаем учащихся к высказыванию собственного мнения относительно смысла, заключенного в эпиграфе к уроку, и подводим их к мысли, что при выполнении практической работы очень важен навык наблюдения, гак как на основе наблюдений осуществляется основополагающая часть эксперимента, а именно вывод. | Высказывают собственную точку зрения и аргументируют ее. Определяются относительно целей урока. Высказывают свою точку зрения на идею эпиграфа. |
Актуализация ЗУН | Химические реакции, призн химических химические уравнения, коэффициент, | Предлагаем учащимся выполнить тест. Организуем активное обсуждение результатов теста и коррекции знаний. Проводим беседу с учащимися о мерах безопасности при работе с оборудованием и реактивами: Работа со стеклом; Правила работы со спиртовкой; Обращение с кислотами, а также оксидами и солями | Выполняют тест, осуществляют самопроверку и корректировку знаний. Слушают, отвечают на вопросы учителя. | |
Выполнение эксперимента | Наблюдение различных признаков химических реакций при проведении | Предлагаем выполнить практическую работу согласно инструкции. Наблюдаем за выполнением работы , при необходимости помогаем или консультируем. | Выполняют практическую работу, оформляют результаты работы, сдают работу учителю. | |
Рефлексия | Результат и деятельность | Предлагаем учащимся высказать мнение относительно полученных результатов | По желанию отвечают на вопрос, высказывая мнение, о достигнутом результате и о том, что способствовало его достижению(или помешало достижению большего). | |
Домашнее задание | Повторить материал §24. с. 124-128 | Предлагаемый для домашней работы материал необходим для выполнения работы по приготовлению раствора с определенной массовой долей вещества | Задают вопросы на уточнение |
Тест для актуализации знаний и умений
Тест может быть предложен как контрольно - актуализирующий на данном уроке или на последующем. Ответы вносятся в специальный бланк, результаты работы собираем через несколько минут, и после этого предлагаем учащимся осуществить и откорректировать знания. Результат теста учитываем при выставлении отметки за работу или как отдельный вид работы с отдельной оценкой
Тест Внимание!
Вариант - 1.
1 . Химические явления – это превращения веществ, когда
а) изменяется агрегатное состояние и форма;
б) изменяется состав вещества;
в) изменяется размер и масса;
г) изменяется цвет;
2. Химические явления можно условно записать с помощью
а) физических формул;
б) математических уравнений;
в) химических уравнений;
г) химических знаков
3. Коэффициент - это
а) химический знак;
в) химическая формула:
4.Укажите признаки химической реакции
а) изменение цвета:
б) изменение формы и размера;
в) выделение тепла (или света);
г) образование осадка и газа
5. Реакция между простым и сложным веществом, как правило, является реакцией
а) соединения; б) замещения;
в) разложения; г) обмена
Тест Внимание! Верных ответов может быть несколько.
Вариант-2
1. Химические явления - это
а) горение газа; б) испарение воды;
в) гниение листьев;
г) перегонка нефти;
2. Химические уравнения составляются на основе
а) периодического закона;
б) закона постоянства состава Ж. Пруста;
в) закона сохранения массы веществ;
г) закона Авогадро
3. Индекс - это
а) химический знак;
б) цифра, стоящая перед формулой или химическим знаком;
в) химическая формула;
г) цифра, стоящая возле химического знака справа внизу
4.Образование осадка, появление запаха, выделение тепла, света, газа, изменение цвета - это
а) превращения веществ:
б) свойства веществ;
в) признаки химических реакций;
г) физические явления:
5.Реакция, при которой из нескольких веществ образуется новое более сложное вещество, называется реакцией
а) соединения;
б) разложения;
в) обмена;
г) замещения;
Этапы работы | Выполнение опыта | Наблюдения | Уравнения реакций, названия продуктов | |
|
Взаимодействие оксида меди(П) с серной кислотой | ||||
|
Взаимодействие карбоната кальция (мела) с соляной кислотой | СаСОз и НС1 | Наблюдайте цвет, осадок, газ, запах, свет или выделение тепла. | Укажите наблюдаемые признаки данной реакции и её тип. |
|
|
Взаимодействие хлорида железа (III) с роданидом калия | Наблюдайте цвет, осадок, газ. запах, свет или выделение тепла. | Укажите наблюдаемые признаки данной реакции и её тип. |
||
|
Взаимодействие карбоната хлоридом | Na 2C03 и СаСl2 | Наблюдайте цвет, осадок, газ. запах. свет или выделение тепла. | Укажите наблюдаемые признаки данной реакции и её тип. |
А. Нарисуйте на одной из ступенек лесенки человечка - себя, в зависимости от вашей активной работы на уроке:
https://pandia.ru/text/78/636/images/image003_129.gif" height="38"> 3
Б. Поставьте отметку рядом с одним из значков в первом столбце:
На уроке всё понятно |
|
Осталось ощущение, что понятно не все |
|
Всё было понятно, я смогу сам (а) проводить опыты и наблюдать признаки их сопровождающие. |
В
. Выберите себе понравившееся начало предложения и допишите его
1 .Сегодня узнал (а), что могу -----
2. Я считаю полезным
3. Мне понравилось -
4. Мне было трудно
5. Теперь бы я хотел (а) ещё узнать-------
Домашнее задание: повторить материал §24. с. 124-128
Бланк для ответов
Класс Ф. И Сумма баллов Оценка |
|||||
На протяжении всей жизни мы постоянно сталкиваемся с физическими и химическими явлениями. Природные физические явления для нас столь привычны, что мы уже давно не придаём им особого значения. Химические реакции постоянно протекают в нашем организме. Энергия, которая выделяется при химических реакциях, постоянно используется в быту, на производстве, при запуске космических кораблей. Многие материалы, из которых изготовлены окружающие нас вещи, не взяты в природе в готовом виде, а изготовлены с помощью химических реакций. В быту для нас не имеет особого смысла разбираться в том, что же произошло. Но при изучении физики и химии на достаточном уровне без этих знаний не обойтись. Как отличить физические явления от химических? Существуют ли какие-либо признаки, которые могут помочь это сделать?
При химических реакциях из одних веществ образуются новые, отличные от исходных. По исчезновению признаков первых и появлению признаков вторых, а также по выделению или поглощению энергии мы заключаем, что произошла химическая реакция.
Если прокалить медную пластинку, на её поверхности появляется чёрный налёт; при продувании углекислого газа через известковую воду выпадает белый осадок; когда горит древесина, появляются капли воды на холодных стенках сосуда, при горении магния получается порошок белого цвета.
Выходит, что признаками химической реакций являются изменение окраски, запаха, образование осадка, появление газа.
При рассмотрении химических реакций, необходимо обращать внимание не только на то, как они протекают, но и на условия, которые должны выполняться для начала и течения реакции.
Итак, какие же условия должны быть выполнены для того, чтобы началась химическая реакция?
Для этого прежде всего необходимы реагирующие вещества привести к соприкосновению (соединить, смешать их). Чем более измельчены вещества, чем больше поверхность их соприкосновения, тем быстрее и активнее протекает реакция между ними. Например, кусковой сахар трудно поджечь, но измельчённый и распылённый в воздухе он сгорает за считанные доли секунды, образуя своеобразный взрыв.
С помощью растворения мы можем раздробить вещество на мельчайшие частицы. Иногда предварительное растворение исходных веществ облегчает проведение химической реакции между веществами.
В некоторых случаях соприкосновение веществ, например, железа с влажным воздухом, достаточно, чтобы произошла реакция. Но чаще одного соприкосновения веществ для этого недостаточно: необходимо выполнение ещё каких-либо условий.
 Так, медь не вступает в реакцию с кислородом воздуха при невысокой температуре около 20˚-25˚С. Чтобы вызвать реакцию соединения меди с кислородом, необходимо прибегнуть к нагреванию.
Так, медь не вступает в реакцию с кислородом воздуха при невысокой температуре около 20˚-25˚С. Чтобы вызвать реакцию соединения меди с кислородом, необходимо прибегнуть к нагреванию.
На возникновение химических реакций нагревание влияет по – разному. Для одних реакций требуется непрерывное нагревание. Прекращается нагревание – прекращается и химическая реакция. Например, для разложения сахара необходимо постоянное нагревание.
В других случаях нагревание требуется лишь для возникновения реакции, оно даёт толчок, а далее реакция протекает без нагревания. Например, такое нагревание мы наблюдаем при горении магния, древесины и других горючих веществ.
сайт, при полном или частичном копировании материала ссылка на первоисточник обязательна.